国家食品药品监督管理总局(下称“食药总局”)近日发布的针对美可高特(中国)羊乳有限公司食品安全审计主要问题的通告指出,美可高特(中国)羊乳有限公司主要管理技术人员掌握食品安全法律法规及生产许可相关知识不足,甚至涉嫌编造检验记录。《经济参考报》记者2月27日就整改以及停产情况致电美可高特公司,但截至记者发稿前并未得到任何回复。
2015年12月,国食药总局组织食品安全审计工作组,依据国家相关法律规定,对美可高特(中国)羊乳有限公司的生产许可条件保持情况、食品安全管理制度落实情况以及国家监督抽检不合格产品的追溯、召回、处置情况进行了食品安全审计。据悉,此次审计的原因是,2015年8月,美可高特生产的“美可高特”牌配方羊奶粉检出阪崎肠杆菌。食药总局相关人员介绍说,阪崎肠杆菌是存在于环境中的一种致病菌,对0至6月龄婴儿,尤其是早产儿、低体重儿以及免疫力缺陷婴儿存在较高健康风险。按食品安全国家标准规定,阪崎肠杆菌在婴儿配方乳粉中不得检出。
美可高特公司官网显示,其是集生产婴幼儿系列羊奶粉、孕产妇系列羊奶粉、大众系列羊奶粉、礼盒装羊奶粉等为一体的羊乳制品生产企业。目前,在全国有其天津西青、天津静海、陕西渭南、陕西富平四大基地。2011年,美可高特获得软银赛富三期的1500万美元投资基金,是国际资本青睐并投资的国内唯一的羊奶企业。食药总局在去年12月的审计中发现,美可高特公司部分生产场所、设备设施未持续保持生产许可条件;食品安全管理制度落实不到位;硒、碘、亚油酸、维生素D和三聚氰胺的检验能力不足,不符合GB23790—2010中10.1条款关于检验能力的要求;存在微生物污染风险。而其中最为严重的是,美可高特公司生产记录不完整、检验记录不真实。食药总局表示,美可高特公司未能提供库房内存放的净含量均为120克的白罐婴儿配方乳粉(生产日期为2015年8月4日)、白罐较大婴儿配方乳粉(生产日期为2015年9月22日)、白罐幼儿配方乳粉(生产日期为2015年9月22日)共3批次产品的生产、检验记录,不符合GB23790—2010中15.1条款关于对生产、检验等环节详细记录的要求。而编号为150140的成品检验报告的批准日期为2015年1月30日,但该报告中微生物检验记录完成日期为2015年1月31日,核苷酸检验记录完成日期为2015年2月3日;抽查的多份检验原始记录中,“水分”项目的平行称量数据完全一致;2015年1月—6月,阪崎肠杆菌和沙门氏菌所用培养基的采购量(16瓶,250g/瓶)与实际检验培养基需求量(43瓶,250g/瓶)不匹配,不符合GB23790—2010中15.1条款关于如实记录产品检验情况的要求,涉嫌编造检验记录。“天津市食品药品监督管理部门已责令美可高特(中国)羊乳有限公司停产整改,并且食药总局要求天津市食品药品监督管理部门对美可高特(中国)羊乳有限公司涉嫌编造检验记录情况进一步开展调查,依法处理。”食药总局相关人士表示。
更多精彩资讯>>>

 猜你喜欢
猜你喜欢 数据显示:2021年国庆档新上
数据显示:2021年国庆档新上 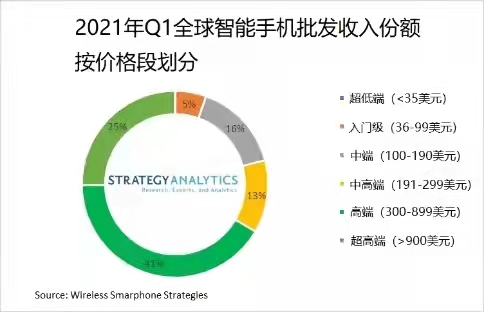 苹果、三星分食高端市场利润
苹果、三星分食高端市场利润  微信拟推出聊天记录付费云存
微信拟推出聊天记录付费云存  个人养老金制度加速崛起 金
个人养老金制度加速崛起 金  飞猪回应 “环球优速通被自
飞猪回应 “环球优速通被自  前8个月全国固定资产投资两
前8个月全国固定资产投资两  坚持公益 初心不改 ——华
坚持公益 初心不改 ——华  质保索赔、官网均关闭 卖了
质保索赔、官网均关闭 卖了